
신약 개발의 생산성 문제와 대안으로서 AI
알파고로(AlphaGo) 혁신을 알린 AI 기술은 2020년 AlphaFold2로 신약 개발 영역으로의 확장을 선포하였다. 알파폴드2의 단백질 구조예측 능력은 실제 실험적으로 밝혀진 결과와 거의 유사한 수준까지 이르러, 신약 개발의 첫 관문인 타깃 단백질의 구조 분석 연구에 널리 활용되고 있다(그림 1). 특히 이러한 단백질 구조예측 및 디자인을 통한 신약 개발은 저분자화합물부터 바이오의약품 개발에 이르기까지 확장되었다.
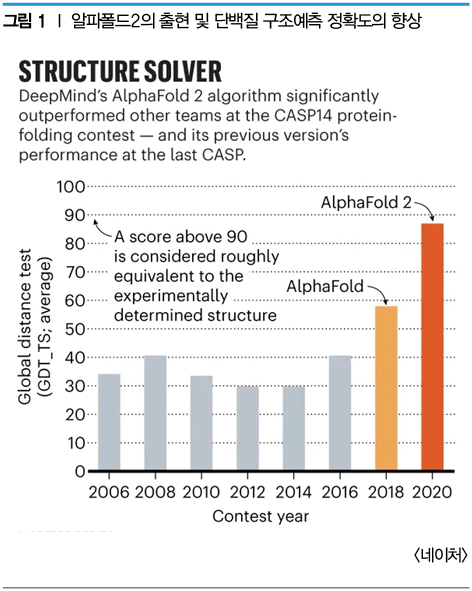
신약 개발은 가장 대표적인 high risk high return 분야로, 비용과 시간이 많이 소요되나 성공률이 매우 낮다. 이에 연구자들은 헤아릴 수 없는 시행착오를 겪는데, 예를 들어 1/5,000~1/10,000 이하로 한 화합물이 임상 1상 시험에 진입할 확률은 10%도 되지 않는다. 임상 1상부터 시판 승인까지 받을 확률 역시 10% 수준이다. 또한 글로벌 상위 제약사 기준으로 신약 개발에 평균 15년, 연구비는 약 3조 원이 소요되었다. 이러한 문제점으로 인해 다국적 제약 기업의 평균 투자 대비 수익률은 2010년에 약 10%였으나 2019년에는 2% 미만으로 떨어지는 등, 신약 개발의 생산성 저하 문제는 심화하고 있다.
이렇게 심각한 신약 개발의 생산성 저하 문제를 해결할 수 있는 가장 적절한 방법은 자율화, 자동화 및 의사결정 지원이 가능한 AI 기술일 것이다. 한국보건산업진흥원의 자료에 의하면 AI 기술을 신약 개발에 적용할 경우, 개발 기간을 7년 단축하고 약 6,000억 원의 비용을 절감할 수 있다. 국내 AI 기술은 글로벌 6위 수준의 상당한 역량을 확보하고 있으며, 특히 국내 제약바이오산업은 지난 1998년 첫 국산 신약을 개발한 이래 25년간 총 36개의 국산 신약을 개발한 저력을 보여주고 있다. 이처럼 글로벌 경쟁력을 확보한 AI 기술과 신약 개발 역량을 접목하여, 신약 개발 산업을 어떻게 하면 반도체를 이을 차세대 산업으로 발전시킬 것인지에 관해 논해보고자 한다.
신약 개발에의 AI 도입 현황 및 활용 사례
AI를 통한 신약 개발의 첫 성공 사례는 중국 Insilico Medicine사의 성과가 2019년 Nature Biotechnology에 발표되면서 알려졌다. 이들은 DDR1 kinase 타깃 저해제로 특발성폐섬유증(IPF) 동물모델에서 효과적인 선도물질을 불과 46일 만에 발굴했으며, 2023년 7월에는 시험 물질 INS018_055로 IPF 환자 대상의 임상 2상을 개시했다. 또한 지난 코로나 팬데믹 기간에 영국 Benevolent사는 기승인받은 EliLilly사의 류마티스 관절염 치료제 Baricitinib(JAK 저해제)이 코로나19 치료제로서 효과적일 것이라고 예측했고, 마침내 2022년 6월 FDA 승인을 받았다. 이는 AI로 기존 약물의 새로운 적응증을 창출한 첫 성공 사례가 되었다. 또한 Icosavax사는 AI로 설계한 단백질을 이용하여 백신을 제조한 성공 사례도 발표하였다. 이 외에도 다음 신약 개발 단계별로 다양한 성공 사례가 만들어지고 있다(그림 2).
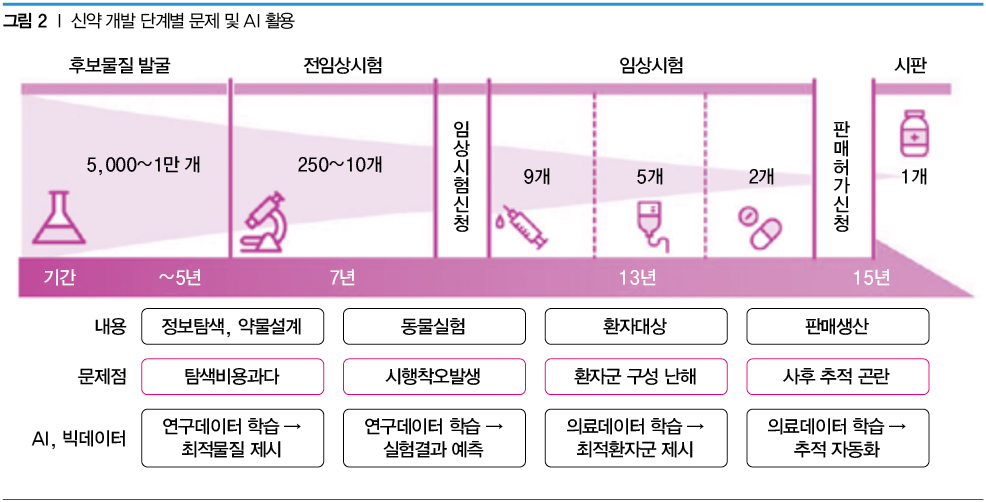
1) 약물 표적의 발견: 2023년 3월 AstraZeneca는 영국의 AI 회사인 Benevolent와 협력 연구하여, IPF의 잠재 표적으로 혈청 반응 인자(SRF)에 대한 전임상 결과를 발표했다. 이 결과에서 SRF에 의한 전사 억제가 잠재적으로 IPF에서 항 섬유 효능을 나타낼수 있음이 밝혀졌다.
2) 표적 기반 약물의 발견: 2023년 초 BMS와 Exscientia는 계획된 세 가지 후보 중 첫 번째를 발전시켰다. 이는 2019년 3월 초기 AI 기반 협력으로 PKC-세타 억제제 EXS4318를 최초의 임상 후보로 도출한 사례이다.
3) 임상시험 설계: 2023년 3월 GSK와 PathAI는 임상시험 설계 역량 강화를 위한 협력을 발표했다. 임상 2a 시험에서는 NASH 및 진행성 섬유증 환자를 대상으로 위약과 비교하여, GSK4532990 물질의 간 섬유증 및 염증 개선의 정도를 측정할 계획이다. 이 과정 중 무작위 대조 임상시험에 PathAI의 AI 기반 NASH 조직학 측정 도구(AIM-NASH)를 활용하여 병리학자도 지원한다는 구상이다.

국내·외 AI 신약 개발 강화 노력
미국 FDA는 신약 개발 전 단계에서 AI 사용이 증가하고 있음을 인식하며 관련 의견서를 발표했다(표 1). 유럽의 경우, 2019년 머신러닝 기반의 신약 개발 프로젝트인 MELLODDY(Machine Learning Ledger Orchestration for Drug Discovery)를 통해 10개 제약사 간 협력 모델을 제시하고 신약 개발의 가속화 및 효율화를 강화하고자 했다. 2022년 대규모 AI 플랫폼의 운영은 단일 파트너 모델에 비해 예측 성능에서 더 뛰어난 성과를 나타냈으며, 약물 후보 물질 설계 및 의사결정 프로세스 지원도 우월하다는 결과가 발표되었다. 국내에서도 한국보건산업진흥원과 한국제약바이오협회가 2018년 ‘AI 신약 개발지원센터’를 설립했다.
2024년에는 보건복지부와 과학기술정보통신부가 공동으로 한국형 연합학습(Federated Learning) 기반 신약 개발 플랫폼인 ‘K-멜로디(K-ELLODDY)’ 사업을 추진한다. 각 제약사, 바이오텍, 연구소, 병원, 학교에 분산된 데이터를 중앙 플랫폼에 집적하여 공용 AI 모델을 개발하고, 이를 신약 개발 프로젝트에 활용하고자 준비 중이다.
미래 신약 개발 분야의 AI 활용 전망
딜로이트의 발표에 따르면, 미래에는 AI가 생명과학 데이터 분석과 패턴 인식을 통해 새로운 바이오마커(biomarker)를 파악하는 데 큰 역할을 할 수 있다. 이는 신약 개발 프로세스의 가속화를 실현해, 생명과학 회사들이 혁신적 치료법을 더 빨리 발견하고 신약을 시장에 더 빨리 출시하는 데 기여할 것이다. 또한 AI로 파악된 화합물의 수가 늘어남에 따라 특정 병리학을 다룰 수 있는 약의 가용성이 증가할 것이다. 질병 메커니즘에 대한 높은 수준의 지식으로 인해 더 많은 치료가 가능해지고, 이전에는 효과적인 치료법이 없었던 질병을 치유하게 될 수 있다.
이러한 전환은 건강산업을 위한 새로운 미래를 열어 줄 것이다. 신약 개발이 점점 더 높은 비율로 가상환경에서 진행되고 선별에서 사전 임상시험까지의 기간이 수개월로 단축되며, 가능성 있는 새로운 약품 후보들이 점차 더 저렴한 비용으로 파악될 것이다. 향후 10년간, 환자들은 이러한 발전이 치료 옵션의 효과와 질병 경과, 특히 현재 치료법이 없는 영역에서 큰 영향을 끼치리라 기대할 수 있다. 이렇듯 우리는 AI를 통해 신약 개발의 전 분야에서의 혁신이 진행되면서 신약 개발 생산성을 대폭 향상시킬 수 있게 되었고, 신약 개발 품목의 다양화(저분자 의약품, 바이오 의약품, 디지털 치료제 등) 및 환자 맞춤형 정밀 의약 발전에 더 빨리, 정확히 다가갈수 있게 될 것이다.





